МІНІ АГЛЯД
Фарпост супраць рака: універсальныя маркеры толькі супраць рака
Чэнчэнь Цянь1, Сяолун Цзоу2, Вэй Лі1,3, Іньшань Лі4, Вэньцян Ю5
1Shanghai Epiprobe Biotechnology Co., Ltd, Шанхай 200233, Кітай;2-е аддзяленне агульнай хірургіі Першай афіляванай бальніцы Харбінскага медыцынскага універсітэта, Харбін 150001, Кітай;3Shandong Epiprobe Medical Laboratory Co., Ltd, Heze 274108, Кітай;4 Народная бальніца Нінся-Хуэйскага аўтаномнага раёна, медыцынскі універсітэт Нінся, Іньчуань 750002, Кітай;5Шанхайскі клінічны цэнтр грамадскага аховы здароўя і аддзяленне агульнай хірургіі, бальніца Хуашань і Інстытут метастазаў рака і лабараторыя эпігенетыкі РНК, Інстытуты біямедыцынскіх навук, Шанхайскі медыцынскі каледж, Універсітэт Фудань, Шанхай 200032, Кітай
АФЕРАТ
Рак з'яўляецца галоўнай прычынай смерці ва ўсім свеце.Ранняе выяўленне рака можа знізіць смяротнасць ад усіх відаў раку;аднак эфектыўныя біямаркеры ранняга выяўлення адсутнічаюць для большасці відаў раку.Метыляванне ДНК заўсёды было галоўнай мэтай цікавасці, таму што метыляванне ДНК звычайна адбываецца раней, чым іншыя выяўляюцца генетычныя змены.У ходзе даследавання агульных асаблівасцей рака з выкарыстаннем новай інструкцыі па вызначэнні паслядоўнасці пазіцыянавання для метылявання ДНК з'явілася серыя універсальных толькі ракавых маркераў (UCOM) як важкія кандыдаты для эфектыўнага і дакладнага ранняга выяўлення рака.У той час як клінічная каштоўнасць сучасных біямаркераў рака зніжаецца з-за нізкай адчувальнасці і/або нізкай спецыфічнасці, унікальныя характарыстыкі UCOM забяспечваюць клінічна значныя вынікі.Пацверджанне клінічнага патэнцыялу UCOM пры раку лёгкіх, шыйкі маткі, эндаметрыя і уротелиального рака дадаткова падтрымлівае прымяненне UCOM пры розных тыпах рака і розных клінічных сцэнарах.Фактычна, у цяперашні час прымяненне UCOM актыўна даследуецца з далейшай ацэнкай ранняга выяўлення рака, дапаможнай дыягностыкі, эфектыўнасці лячэння і маніторынгу рэцыдываў.Наступнымі важнымі тэмамі для вывучэння з'яўляюцца малекулярныя механізмы, з дапамогай якіх UCOM выяўляюць рак.Прымяненне UCOM ў рэальных сцэнарыях таксама патрабуе ўкаранення і ўдасканалення.
КЛЮЧАВЫЯ СЛОВЫ
Выяўленне рака;скрынінг на рак;метилирование ДНК;эпигенетика рака;біямаркеры рака
Чаму нам тэрмінова патрэбна новая біямаркеры?
Пасля больш чым стагоддзя барацьбы з ракам рак па-ранейшаму з'яўляецца самай смяротнай біялагічнай пагрозай для чалавецтва.Рак застаецца праблемай аховы здароўя ў свеце: у 2020 годзе было зарэгістравана 19,3 мільёна новых выпадкаў захворвання і амаль 10 мільёнаў смерцяў1. Паводле ацэнак GLOBOCAN1, у 2020 годзе ў Кітаі было дыягнаставана 4,6 мільёна новых выпадкаў раку, што складае 23,7% ад усіх новых выпадкаў раку ў свеце.Акрамя таго, каля 3 мільёнаў смерцяў у Кітаі ў 2020 годзе былі звязаны з ракам, што склала 30% усіх смерцяў ад раку ў свеце1.Гэтая статыстыка паказала, што Кітай займае першае месца па захваральнасці і смяротнасці ад раку.Больш за тое, 5-гадовая выжывальнасць пры раку складае 40,5%, што ў 1,5 разы ніжэй, чым 5-гадовая выжывальнасць у ЗША2,3.Параўнальна больш нізкая выжывальнасць і больш высокі ўзровень смяротнасці ў Кітаі, чым у краінах з больш высокім індэксам чалавечага развіцця, сведчаць аб тым, што тэрмінова неабходная эфектыўная і эканамічна эфектыўная сістэма прафілактыкі і назірання за ракам.Ранняе выяўленне рака - адзін з найважнейшых элементаў у сістэме аховы здароўя.Ранняе выяўленне рака можа палепшыць прагноз і выжывальнасць на ранніх стадыях амаль усіх тыпаў раку4.Паспяховыя стратэгіі скрынінга прывялі да значнага зніжэння ўзроўню захворвання і смяротнасці ад раку шыйкі маткі, малочнай залозы, прамой кішкі і прастаты.
Ранняе выяўленне рака, аднак, не з'яўляецца лёгкай задачай.Даследаванне біялогіі і прагнозу ранняга рака, вызначэнне і праверка надзейных біямаркераў ранняга выяўлення, а таксама распрацоўка даступных і дакладных тэхналогій ранняга выяўлення заўсёды былі самымі вялікімі перашкодамі ў гэтым працэсе4.Дакладнае выяўленне рака дазваляе адрозніць дабраякасныя паразы ад злаякасных, што дапамагае пазбегнуць непатрэбных працэдур і палягчае далейшае лячэнне хваробы.Сучасныя стратэгіі ранняга выяўлення ўключаюць біяпсію з дапамогай эндаскопа, медыцынскую візуалізацыю, цыталогію, імуналагічныя аналізы і тэсты на біямаркеры5-7.З'яўляючыся інтрузіўнай і дарагой, эндаскопная біяпсія нясе вялікую нагрузку ў якасці асноўнай медыцынскай працэдуры, якая абапіраецца на прафесійны персанал.Як і пры цыталогіі, абодва метады скрынінга залежаць ад медыцынскіх работнікаў і заснаваны на асабістым меркаванні з прадукцыйнасцю, далёкай ад ідэальнай8.Наадварот, імуналагічныя аналізы вельмі недакладныя, улічваючы высокі ўзровень прытворнададатных вынікаў.Медыцынская візуалізацыя, як тактыка абследавання, патрабуе дарагога абсталявання і спецыяльных тэхнікаў.Такім чынам, медыцынская візуалізацыя вельмі абмежаваная з-за нізкай даступнасці.Па ўсіх гэтых прычынах біямаркеры аказваюцца лепшым варыянтам для ранняга выяўлення рака.
Перапіска: Іньшань Лі і Вэньцян Ю
Email: liyinshan@nxrmyy.com and wenqiangyu@fudan.edu.cn
ORCID ID: https://orcid.org/0009-0005-3340-6802 і
https://orcid.org/0000-0001-9920-1133
Паступіў у рэдакцыю 22 жніўня 2023 г.;прынята 12 кастрычніка 2023 г.;
апублікавана ў Інтэрнэце 28 лістапада 2023 г.
Даступна на сайце www.cancerbiomed.org
©2023 Біялогія і медыцына рака.Creative Commons
Міжнародная ліцэнзія Attribution-NonCommercial 4.0
Біямаркеры ў цяперашні час класіфікуюцца як вавёркі, маркеры мутацыі ДНК, эпігенетычныя маркеры, храмасомныя анамаліі, РНК-маркеры, атрыманыя непасрэдна з пухлін, або фрагменты пухлін, атрыманыя ўскосна з вадкасцей арганізма.Бялковыя маркеры - найбольш шырока выкарыстоўваюцца біямаркеры ў скрынінгу і дыягностыцы рака.Бялковыя біямаркеры, як скрынінгавыя біямаркеры, абмежаваныя тэндэнцыяй да дабраякасных паражэнняў, што прыводзіць да празмернай дыягностыкі і празмернага лячэння, як паведамлялася для α-фетапратэіна і прастатычнага спецыфічнага антыгена (ПСА)9,10.РНК-маркеры ўключаюць генетычныя патэрны экспрэсіі і іншыя некадуючыя РНК-маркеры. Камбінацыю маркераў генетычнай экспрэсіі РНК можна выявіць з дапамогай узораў мачы, адчувальнасць якіх была далёкая ад здавальняючай (60%) для першасных пухлін і выяўленне якіх можа быць пад уплывам прыроды лёгкай дэградацыі РНК у нармальным асяроддзі11.Генетычныя і эпігенетычныя маркеры сутыкаюцца з праблемай распаўсюджанасці пухлін і абмежавання тыпамі раку.
Метыляванне ДНК было важкім кандыдатам у якасці біямаркера ранняга выяўлення пасля таго, як Фейнберг у 1983 г. упершыню звязаў яго з ракам12. Аберацыі метылявання ДНК назіраюцца на ўсіх стадыях рака, нават на стадыі перадраку.Аберрантное гиперметилирование ДНК звычайна адбываецца на астраўках CpG у прамотарах генаў, каб супрацьстаяць супрессорам пухліны 13,14.Даследаванні таксама выказалі здагадку, што анамальнае гіперметыляванне ДНК вядзе да павышэння рэгуляцыі рэгулятараў развіцця15.Даліна метылявання ДНК, якая звычайна асацыюецца з рэгулятарамі развіцця і гіперметыляванымі ракавымі захворваннямі, можа пераключыць рэжым экспрэсіі генаў на больш стабільны рэжым, які залежыць ад метылявання ДНК, і паменшыць сувязь з метыляваным гістонам H3K27me3 і звязанымі з ім вавёркамі поликомба16,17.
Сярод вялікай колькасці апублікаваных маркераў метылявання ДНК некалькі паспяхова дэбютавалі на рынку;аднак цяперашнія камерцыялізаваныя маркеры метылявання ДНК і дыягнастычныя панэлі яшчэ не цалкам раскрылі патэнцыял ранняга выяўлення рака па розных прычынах18.У той час як у асноўным паказваюць прымальную прадукцыйнасць з выкарыстаннем інфармацыі з базы дадзеных, гэтыя біямаркеры звычайна працуюць менш ідэальна ў рэальным свеце з-за таго, што рэальныя ўзоры часта больш складаныя і не такія рэпрэзентатыўныя, як выбраныя ў базах дадзеных.Было паказана, што ранняе выяўленне метылявання некалькіх ракаў на аснове секвенавання наступнага пакалення мае толькі 16,8% і 40,4% адчувальнасць пры раку I і II стадыі адпаведна19.Тэсты ранняга выяўлення патрабуюць большай стабільнасці і больш дакладных біямаркераў.
Выяўленне толькі універсальнага маркера рака (UCOM) з выкарыстаннем паслядоўнасці пазіцыянавання (GPS)
Нягледзячы на дзесяцігоддзі даследаванняў рака, здавальняючая прафілактыка і лячэнне не былі рэалізаваны.Новыя метадалогіі неабходныя, каб даць магчымасць даследчыкам старанна ацэньваць рак.За апошнія 23 гады 6 характэрных прыкмет рака, такіх як пазбяганне апоптозу, інвазія ў тканіны і метастазы і г.д., былі пашыраны да 14 за кошт уключэння такіх функцый, як немутацыйнае эпігенетычнае перапраграмаванне і паліморфныя мікрабіёмы20,21.Па меры раскрыцця большай колькасці дэталяў, звязаных з ракам, у даследаванні рака адкрываецца больш перспектыў.Даследаванні рака паступова ўвайшлі ў новую эпоху ў двух напрамках (агульнасць і індывідуальнасць).З развіццём прэцызійнай анкалогіі ў апошнія гады ў цэнтры ўвагі даследаванняў рака схіляюцца да індывідуальнай таргетнай тэрапіі і гетэрагеннасці раку22.Такім чынам, нядаўна ідэнтыфікаваныя біямаркеры рака сканцэнтраваны ў асноўным на пэўных тыпах рака, такіх як PAX6 forcervical рак23 і BMP3 для колоректального рака24.Прадукцыйнасць гэтых біямаркераў, характэрных для тыпаў раку, адрозніваецца, але для адчувальных асоб усё яшчэ немагчыма прайсці абследаванне на ўсе віды раку адначасова з-за абмежавання збору біялагічных узораў і высокага кошту.Было б ідэальна, калі б мы змаглі вызначыць адзіны надзейны біямаркер, эфектыўны для ўсіх відаў раку на ранняй стадыі.
Каб дасягнуць такой ідэальнай мэты, трэба выбраць лепшага кандыдата ў біямаркеры са спісу патэнцыйных тыпаў біямаркераў.Аберацыі метылявання ДНК сярод усіх генетычных і эпігенетычных профіляў, як вядома, звязаныя з ракам і з'яўляюцца аднымі з самых ранніх, калі не першымі, анамаліямі, звязанымі з ракам, якія ўзнікаюць у храналагічным парадку.Даследаванне метылявання ДНК пачалося рана, але яму перашкаджала адсутнасць метадаў даследавання.Сярод 28 мільёнаў патэнцыйных метыляваных сайтаў CpG у геноме неабходна выявіць кіраваную колькасць і супаставіць іх з геномам, каб лепш зразумець адукацыю пухлін.Бісульфітнае секвеніраванне поўнага геному (WGBS), якое лічыцца залатым стандартам секвеніравання метылявання ДНК, можа ахапіць толькі 50% Cs у ракавых клетках з-за характару лячэння бісульфітам, які разбівае фрагменты ДНК і зніжае складанасць геному падчас ператварэнне Цс-у-Ц25.Іншыя метады, такія як 450 тыс. мікрасхем, ахопліваюць толькі 1,6% метылявання геному.На падставе 450 тыс. дадзеных панэль выяўлення метылявання ДНК мае 35,4% адчувальнасці для 6 тыпаў раку I стадыі26.Абмежаванні тыпаў раку, нізкая прадукцыйнасць і шум, які ствараецца метадамі выяўлення ў аналітычным працэсе, сталі самымі вялікімі перашкодамі для панэляў выяўлення раку.
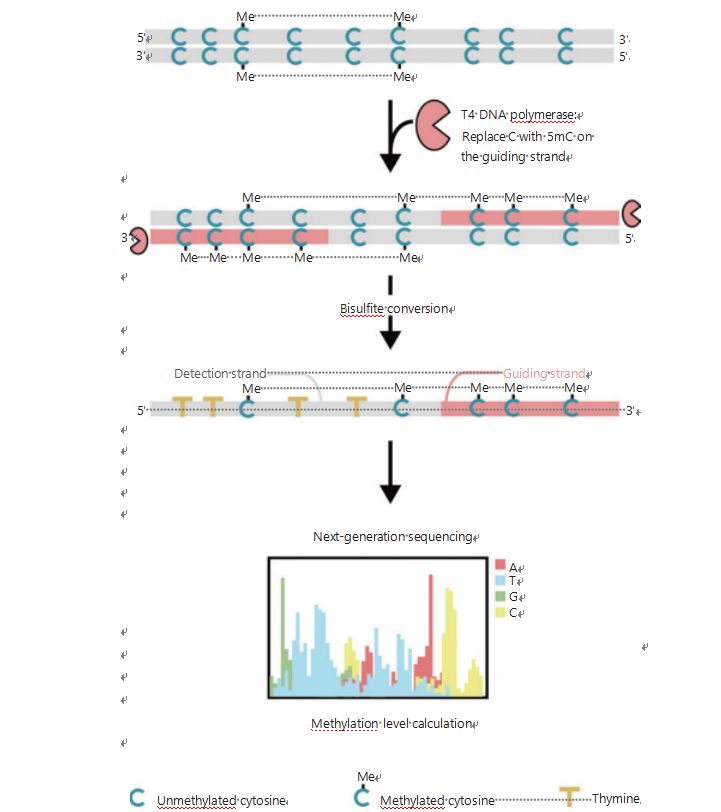
Каб лепш даследаваць эпігенетычныя заканамернасці клетак падчас опухолеобразования і метастазірованія, мы распрацавалі унікальны GPS для выяўлення метылявання ДНК у геноме, які ахоплівае да 96% сайтаў CpG за 0,4 мільярда чытанняў25.GPS - гэта двухбаковы метад секвеніравання з выкарыстаннем 3'-канца фрагмента ДНК неканверсоўных метылацытазінаў пасля апрацоўкі бісульфітам, які накіроўвае выраўноўванне вылічэнняў метылявання ДНК 5'-канца праз парнае секвеніраванне (малюнак 1)25.Накіроўваючы ланцуг метылцытазіну, які дзейнічае як шаблонны ланцуг, дапамагае ў выраўноўванні вобласці з высокім GC, што аднаўляе найбольш закінутыя дадзеныя секвеніравання ў традыцыйным WGBS.Функцыя GPS з высокім ахопам дае велізарную колькасць інфармацыі аб метыляванні ДНК, што дазваляе нам даследаваць профілі метылявання рака са значна больш высокім дазволам у раней недастаткова даследаваных рэгіёнах.
GPS дае нам магутны інструмент для даследавання аднастайнасці раку, які можа значна спрасціць даследаванне рака і патэнцыйна знайсці універсальнае тлумачэнне адукацыі пухлін і метастазаў.Пры аналізе GPS-дадзеных ліній ракавых клетак часта сустракаўся унікальны феномен.У розных тыпах ракавых узораў быў шэраг абласцей, якія аказваліся анамальна гіперметыляванымі.Гэтая нечаканая знаходка была пасля пацверджана, каб служыць UCOM.Было прааналізавана больш за 7000 узораў з 17 тыпаў раку ў базе дадзеных Атласа геному рака (TCGA), сярод якіх мы ідэнтыфікавалі першы UCOM, HIST1H4F, ген, звязаны з гістонам, які гіперметыляваны ва ўсіх тыпах раку27.Серыя UCOM была затым знойдзена і праверана ў базе дадзеных TCGA, базе дадзеных Gene Expression Omnibus (GEO) і рэальных клінічных узорах.На дадзены момант HIST1H4F, PCDHGB7 і SIX6 былі знойдзены і пацверджаны як UCOM.Нечаканае адкрыццё UCOM прапануе магутны адказ на неабходнасць ранняга выяўлення рака.UCOM забяспечваюць рашэнне для выяўлення некалькіх відаў раку па адным маркеру.
Характарыстыка УКОМ
Пасля праверкі было паказана, што UCOMs дэманструюць чатыры асноўныя характарыстыкі, якія дазваляюць UCOMs перасягнуць эфектыўнасць сучасных біямаркераў (мал. 2).
Унікальны для злаякаснай пухліны
UCOM з'яўляюцца ўнікальнымі для ракавых або предраковых пашкоджанняў і на іх не ўплываюць звычайныя фізіялагічныя змены.Некаторыя з сучасных маркераў, звязаных з ракам, якія шырока выкарыстоўваюцца для ранняга выяўлення і/або скрынінга, прывялі да гіпердыягностыкі.Павышаны ўзровень ПСА, клінічна акрэдытаваны інструмент скрынінга, таксама выяўляецца пры дабраякасных захворваннях, такіх як гіперплазія прастаты і прастатыт10.Залішняя дыягностыка і адпаведнае празмернае лячэнне прыводзяць да зніжэння якасці жыцця з-за кішачных, мачавых і сэксуальных ускладненняў28.Іншыя заснаваныя на бялку і шырока выкарыстоўваюцца ў клінічных умовах біямаркеры, такія як CA-125, не прынеслі істотных пераваг, хоць выклікалі празмерную дыягностыку і празмернае лячэнне29.Высокая спецыфічнасць UCOM для злаякасных пухлін дазваляе пазбегнуць гэтых недахопаў.UCOM, PCDHGB7, эфектыўна адрознівае плоскія ўнутрыэпіцеліальныя паразы высокай ступені (HSIL) і рак шыйкі маткі ад нармальных узораў і нізкаякасных плоскіх унутрыэпіцеліяльных паражэнняў (LSIL), у той час як большасць іншых біямаркераў могуць толькі адрозніць рак шыйкі маткі ад нармальных узораў30.Нягледзячы на тое, што PCDHGB7 не выяўляе значных адрозненняў паміж нармальным эндаметрыем і гіперплазіяй эндаметрыя, значныя адрозненні выяўляюцца паміж нармальным эндаметрыем і атыповай гіперплазіяй, і яшчэ большыя адрозненні выяўляюцца паміж нармальным эндаметрыем і ракам эндаметрыя (EC) на аснове PCDHGB731.UCOMs з'яўляюцца унікальнымі для злаякасных паражэнняў у базах дадзеных і клінічных пробах.З пункту гледжання пацыента, унікальныя UCOM зніжаюць парог для разумення складаных прыкмет розных неэфектыўных нестабільных біямаркераў і адпаведнай трывогі ў працэсе ацэнкі.З пункту гледжання клініцыста, унікальныя UCOM адрозніваюць злаякасныя пухліны ад дабраякасных, што дапамагае ў сартаванні пацыентаў і памяншае непатрэбныя медыцынскія працэдуры і празмернае лячэнне.Такім чынам, унікальныя UCOM памяншаюць празмернасць медыцынскай сістэмы, палягчаюць сістэмны дыстрэс і робяць даступнымі больш медыцынскіх рэсурсаў для тых, хто мае патрэбу.
Малюнак 1. Схема працоўнага працэсу GPS для выяўлення метылявання ДНК25.Шэрая лінія: уваходная паслядоўнасць ДНК;чырвоная лінія: ДНК, апрацаваная ДНК-палімеразай Т4, з заменай цытазіну на 5'-метилцитозин на 3'-канцы ўваходу;сіні C з Me: метилированный цитозин;сіні C: неметилированный цитозин;жоўты Т: тымін25.
Усё ці нічога
UCOM прысутнічаюць толькі ў ракавых клетках і стабільна выяўляюцца амаль ва ўсіх ракавых клетках.Было пацверджана, што HIST1H4F гіперметыляваны амаль ва ўсіх тыпах пухлін, але не ў нармальных узорах27.Падобным чынам было паказана, што PCDHGB7 і SIX6 гиперметилированы ва ўсіх узорах пухлін, але не ў нармальных узорах 30-32.Гэтая унікальная характарыстыка істотна паляпшае прадукцыйнасць UCOM у дачыненні да мяжы выяўлення і адчувальнасці.Усяго толькі 2 % ракавых клетак можна дыферэнцаваць ва ўзорах, што робіць UCOM значна больш адчувальным біямаркерам, чым большасць існуючых біямаркераў30. Як біямаркер, які выкарыстоўваецца для выяўлення рака прамой кішкі, мутацыі KRAS існуюць толькі прыкладна ў 36 % выпадкаў рака прамой кішкі. што сведчыць аб слабым дыягнастычным патэнцыяле33.Нізкая распаўсюджанасць мутацый KRAS пры колоректальном раку абмяжоўвае KRAS у спалучэнні з іншымі биомаркерами.Фактычна, камбінацыя біямаркераў першапачаткова можа здацца шматспадзеўнай, але не заўсёды дае здавальняючы вынік, адначасова дэманструючы значна большы шум пры аналізе выяўлення і звычайна ўключае ў сябе больш складаныя эксперыментальныя працэдуры.Наадварот, PCDHGB7 і іншыя UCOM існуюць ва ўсіх відах раку.UCOM выяўляюць ракавыя кампаненты ў розных тыпах ракавых узораў з найвышэйшай дакладнасцю, адначасова выкараняючы складаныя працэсы аналізу шумапрыглушэння.Няцяжка выявіць рак у багатай пробе, але вельмі складана выявіць рак у маленькай пробе.UCOM здольныя выяўляць невялікія колькасці рака.
Малюнак 2. Характарыстыкі UCOM.
Выяўленне рака, якое папярэднічае паталагічным зменам
UCOM могуць быць выяўленыя ў предраковые стадыі да паталагічных змен.Як эпигенетические биомаркеры, анамаліі UCOM адбываюцца на больш ранняй стадыі, чым фенатыпічнае анамаліі, і выяўляюцца на працягу пухліннага генезу, прагрэсавання і метастазірованія34,35.Адчувальнасць UCOM з цягам часу павышае прадукцыйнасць UCOM пры выяўленні рака на ранніх стадыях і предраковые паразы.Выяўленне раку на ранняй стадыі на аснове біяпсіі і цыталогіі можа быць цяжкім нават для самых вопытных патолагаанатамаў.Аднаразовая біяпсія, атрыманая пры кольпоскопіі, была прызнана станоўчай у 60,6% узораў HSIL+.Дадатковая біяпсія патрабуецца пры множных паражэннях для павышэння адчувальнасці36.Наадварот, UCOM, PCDHGB7, мае адчувальнасць 82% для ўзораў HSIL+, што перавышае адчувальнасць біяпсіі і большасці біямаркераў30.Маркер метылявання, FAM19A4, мае адчувальнасць 69% для CIN2+, што падобна на цыталогію, але не можа адрозніць CIN1 ад нармальных узораў37.Было паказана, што UCOM з'яўляюцца значна больш адчувальным біямаркерам ранняга выяўлення.У параўнанні з патолагаанатамамі, заснаванымі на вопыце, UCOM валодаюць найвышэйшай адчувальнасцю выяўлення рака на ранніх стадыях, што, у сваю чаргу, спрыяе паляпшэнню прагнозу і выжывальнасці пры раку30.Акрамя таго, UCOMs прапануе платформу выяўлення, якая даступная для раёнаў, дзе не хапае вопытных патолагаанатамаў, і значна павышае эфектыўнасць выяўлення.Дзякуючы аднастайным працэдурам адбору пробаў і выяўлення, выяўленне UCOM дае стабільныя і простыя для інтэрпрэтацыі вынікі, якія лепш адпавядаюць пратаколу скрынінга, які патрабуе менш прафесійнага персаналу і медыцынскіх рэсурсаў.
Лёгка выявіць
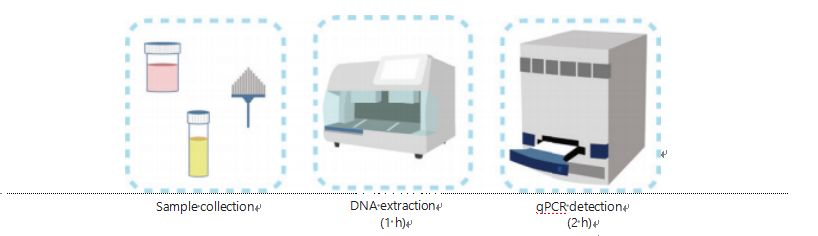
Сучасныя метады выяўлення метылявання ДНК складаныя і займаюць шмат часу.Большасць метадаў патрабуе бісульфітнай трансфармацыі, што прыводзіць да страты якасці ўзору і, магчыма, дае нестабільныя і недакладныя вынікі.Дрэнная ўзнаўляльнасць, выкліканая лячэннем бісульфітам, патэнцыйна прыводзіць да блытаніны для лекараў і пацыентаў і ў далейшым перашкаджае назіранню і/або стратэгіі лячэння.Такім чынам, мы дадаткова змянілі метад выяўлення UCOM, каб пазбегнуць праблематычнай апрацоўкі бісульфітам узораў, улічыць патрабаванні клінічнага прымянення і павысіць даступнасць.Мы распрацавалі новы метад з выкарыстаннем рэстрыкцыйных ферментаў, адчувальных да метылявання, у спалучэнні з флуоресцентной колькаснай ПЦР у рэальным часе (Me-qPCR) для колькаснай ацэнкі статусу метылявання UCOM на працягу 3 гадзін з выкарыстаннем простых працэдур (малюнак 3).Me-qPCR можа змяшчаць некалькі тыпаў узораў, такіх як клінічны збор біялагічных вадкасцей і ўзоры мачы, узятыя самастойна.Сабраныя клінічныя ўзоры можна апрацоўваць, захоўваць і лёгка пераходзіць да выяўлення з дапамогай стандартызаванай і аўтаматызаванай экстракцыі ДНК.Затым вынятую ДНК можна наўпрост нанесці на платформу Me-qPCR для рэакцыі ў адным гаршчку і атрымання вынікаў колькаснага вызначэння.Пасля простага аналізу вынікаў з выкарыстаннем дыягнастычных мадэляў, падагнаных і пацверджаных для пэўных тыпаў раку, канчатковае вызначэнне вынікаў выяўлення UCOM інтэрпрэтуецца і прадстаўляецца ў выглядзе паўколькаснага значэння.Платформа Me-qPCR пераўзыходзіць традыцыйнае бісульфітнае пірасеквеніраванне ў выяўленні UCOM, эканомячы пры гэтым 3 гадзіны пераўтварэння бісульфіту ў адпаведнасці з пратаколам набору EZ DNA Methylation-Gold.Інавацыйная платформа выяўлення метылявання робіць выяўленне UCOM больш стабільным, дакладным і больш даступным30.
Малюнак 3. Працэс выяўлення UCOM.Да тыпаў узораў адносяцца прафесійна ўзятыя пробы БАЛП, чыстка мазка Папаніколау і/або мача, сабраная самастойна.Працэс экстракцыі ДНК можа быць прыстасаваны да аўтаматычнага экстрактара, прадукт якога можна непасрэдна выявіць з дапамогай кПЦР.
Прымяненне UCOMs
Рак лёгкіх
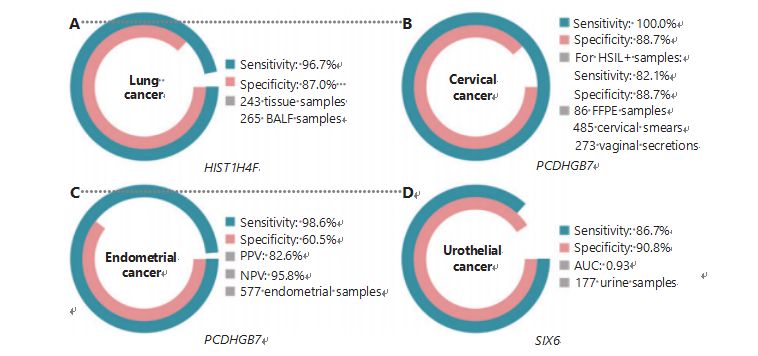
Рак лёгкіх з'яўляецца другім найбольш часта дыягнастуемым і смяротным ракам ва ўсім свеце, на яго долю прыпадае 11,4% новых выпадкаў і 18,0% новых смерцяў1.Сярод усіх дыягназаў 85% складаюць немелкоклеточный рак лёгкага (НМРЛ), а 15% - мелкоклеточный рак лёгкага (МРЛ), які мае больш высокі ўзровень злаякаснасці38.Кампутарная тамаграфія з нізкімі дозамі (LDCT) з'яўляецца ў цяперашні час рэкамендаваным метадам абследавання на рак лёгкага і, як было паказана, паляпшае ранняе выяўленне і зніжае смяротнасць6;аднак, з-за нізкай спецыфічнасці і дрэннай даступнасці, LDCT яшчэ не служыць у якасці здавальняючага метаду скрынінга, як і іншыя распаўсюджаныя маркеры рака, такія як CEA39.Выдаткі і патэнцыял неўстаноўленых дыягназаў і памылковых дыягназаў стратэгіі скрынінга LDCT перашкаджаюць прагрэсу ў прасоўванні скрынінга на рак лёгкіх40.HIST1H4F, UCOM, мае велізарны патэнцыял у якасці біямаркера ранняга выяўлення ў пробах бронхаальвеалярнай вадкасці (БАЛ)27.HIST1H4F гіперметыляваны ў аденокарциноме лёгкіх і плоскоклеточном раку лёгкіх са спецыфічнасцю выяўлення 96,7% і адчувальнасцю 87,0% (малюнак 4A), а таксама з выключнай прадукцыйнасцю пры раку I стадыі27.HIST1H4F мае спецыфічнасць 96,5% і адчувальнасць 85,4% для NSCLC і 96,5% і 95,7% адпаведна для SCLC27.Акрамя таго, узоры васьмі іншых тыпаў раку, уключаючы рак падстраўнікавай залозы і колоректальный рак, пацвердзілі, што HIST1H4F гиперметилирован ва ўсіх васьмі тыпах27.
Рак шыйкі маткі
У 2020 годзе рак шыйкі маткі быў чацвёртым найбольш часта дыягнастуемым анкалагічным захворваннем і чацвёртай прычынай смерці ад раку ў жанчын, на яго долю прыпадала 3,1% новых выпадкаў і 3,4% смерцяў, звязаных з ракам, у свеце1.Каб ліквідаваць рак шыйкі маткі да 2030 года, як прапануе СААЗ, неабходна ранняе выяўленне рака шыйкі маткі.Пры выяўленні на ранняй стадыі 5-гадовая выжывальнасць пры інвазівном раку шыйкі маткі дасягае 92%41.У рэкамендацыях Амерыканскага анкалагічнага таварыства (ACS) для скрынінга рэкамендуецца праводзіць цыталагічныя аналізы шыйкі маткі, першасныя аналізы на ВПЧ або катэсты42.Цыталогія шыйкі маткі з'яўляецца інвазівной і можа выявіць толькі 63,5% выпадкаў CIN2+37.
PCDHGB7, у адрозненне ад гэтага, паказаў сябе значна лепш пры выкарыстанні мазка Папаніколау і похвавых вылучэнняў і можа эфектыўна дыферэнцаваць HSIL ад LSIL на звышранняй стадыі.PCDHGB7 сам па сабе мае адчувальнасць 100,0% і спецыфічнасць 88,7% для раку шыйкі маткі (малюнак 4B) і 82,1% адчувальнасць і 88,7% спецыфічнасць для HSIL+ узораў30.PCDHGB7 таксама мае 90,9% адчувальнасць і 90,4% спецыфічнасць ва ўзорах вагінальнага сакрэту на рак шыйкі маткі, якія значна прасцей сабраць30.У спалучэнні з тэстам на ВПЧ высокай рызыкі (hr) або цыталагічным тэстам Thinprep (TCT) PCDHGB7 мае павышаную адчувальнасць 95,7% і спецыфічнасць 96,2%, значна пераўзыходзячы тэст на hrHPV (20,3%), TCT (51,2%) ), і два разам (57,8%) для рака шыйкі маткі30.Таксама было паказана, што PCDHGB7 гіперметыляваны ў 17 тыпах раку з базы дадзеных TCGA, што паказвае на яго прыдатнасць у сямействе UCOM30.
Малюнак 4 UCOM былі пацверджаны ў чатырох тыпах рака ў буйнамаштабных клінічных даследаваннях.A. Прадукцыйнасць HIST1H4F, UCOM, у выяўленні рака лёгкіх 508 узораў.B. Прадукцыйнасць PCDHGB7, UCOM, у выяўленні рака шыйкі маткі 844 узораў.C. Эфектыўнасць PCDHGB7, UCOM, пры выяўленні рака эндаметрыя ў 577 узорах эндаметрыя па Папаніколау і Тао.D. Прадукцыйнасць SIX6, UCOM, у выяўленні уротелиального рака 177 узораў.
EC
ЭК з'яўляецца адным з самых распаўсюджаных ракавых захворванняў жаночай рэпрадуктыўнай сістэмы ва ўсім свеце, паводле ацэнак, 4,2 мільёна новых выпадкаў і 1% смерцяў, звязаных з ракам, штогод1.Пры паспяховым дыягназе на ранняй стадыі ЭК вылечваецца і мае 95% 5-гадовую выжывальнасць пры раку I стадыі.Пацыенты з такімі сімптомамі, як анамальнае маткавае крывацёк, атрымліваюць перыядычнае клінічнае абследаванне і інвазівные і балючыя працэдуры біяпсіі, нягледзячы на тое, што толькі ў 5%-10% з часам развіваецца EC43.Трансвагінальном УГД, як звычайны метад выяўлення, вельмі ненадзейны з-за яго немагчымасці дыферэнцаваць дабраякасныя змены эндаметрыя ад злаякасных і высокай частаты прытворнададатных вынікаў44.
Было праведзена паралельнае параўнанне сыроватачна CA-125, шырока распаўсюджанага биомаркера EC, і PCDHGB7.Сыроватка CA-125 мела адчувальнасць 24,8%, што сведчыць аб тым, што CA-125 з'яўляецца неадэкватным маркерам для EC, нягледзячы на спецыфічнасць 92,3%31.Выяўленне PCDHGB7 з выкарыстаннем узораў пэндзля Папаніколау дало адчувальнасць 80,65% і спецыфічнасць 82,81% для стадый ECatall, у той час як шчотка Tao мела адчувальнасць 61,29% і спецыфічнасць 95,31%31.Дыягнастычная мадэль PCDHGB7, заснаваная на Me-qPCR, дала адчувальнасць 98,61%, спецыфічнасць 60,5% і агульную дакладнасць 85,5%, пры выкарыстанні ўзораў пэндзляў Pap і Tao (малюнак 4C)31.
Уротелиальный рак
Уратэліяльны рак, які ўключае рак мачавой бурбалкі, нырачнай лаханкі і мачаточніка, быў сёмым найбольш часта дыягнаставаным ракам у 2020 годзе ва ўсім свеце, выклікаючы 5,2% новых выпадкаў і 3,9% смерцяў1.Уратэліяльны рак, больш за 50% з якіх прыпадае на рак мачавой бурбалкі, быў чацвёртым найбольш часта дыягнастуемым ракам у ЗША ў 2022 годзе, на яго долю прыпадала 11,6% новых дыягнаставаных выпадкаў3.Прыкладна 75% выпадкаў раку мачавой бурбалкі класіфікуюцца як неинвазивный рак мачавой бурбалкі, абмежаваны слізістай або падслізістага абалонкай45.Біяпсія пры цыстаскапіі з'яўляецца залатым стандартам для дыягностыкі рака уротелия, якая праводзіцца з дапамогай флюарэсцэнтнай гібрыдызацыі in situ (FISH) і цыталагічных тэстаў.FISH і цыталогія маюць дрэнныя дыягнастычныя характарыстыкі, а цыстаскапія з'яўляецца інтрузіўнай і мае асноўны рызыка пропуску мікрапашкоджанняў, няправільнай інтэрпрэтацыі пашкоджанняў і патэнцыйнага распаўсюджвання або рэцыдыву рака46.Раней пацверджаны UCOM, PCDHGB7, быў таксама паказаны як гиперметилированный пры раку уротелия, з плошчай пад крывой 0,86, што сведчыць аб патэнцыйнай дыягнастычнай магчымасці30.Для далейшай праверкі большай колькасці UCOM і лепшага прыстасавання да большай колькасці тыпаў узораў SIX6, новы UCOM, быў даследаваны і паказаў выдатны дыягнастычны патэнцыял у раннім выяўленні уратэліяльнага рака з выкарыстаннем узораў мачы на платформе Me-qPCR.Выяўленне SIX6 з выкарыстаннем узораў мачы прадэманстравала канкурэнтную адчувальнасць 86,7% і спецыфічнасць 90,8% (малюнак 4D), з'яўляючыся неінвазіўным і лёгкім для атрымання32.Патэнцыял SIX6 у маніторынгу метастазаў і ацэнцы эфектыўнасці лячэння ў цяперашні час даследуецца.
Будучыня і выклікі
UCOMs маюць высокую прадукцыйнасць у дыягнастычным патэнцыяле некалькіх відаў раку, але яшчэ шмат працы.Мы пашыраем спіс UCOM і актыўна правяраем UCOM пры большай колькасці відаў раку, у тым ліку тых, якія традыцыйна цяжка выявіць.Вынікі праверкі з баз даных TCGA дадаткова пацвердзілі прымяненне UCOM пры большай колькасці відаў раку і ў большай колькасці сітуацый.У ходзе папярэдняга расследавання было паказана, што UCOM валодаюць надзейным дыягнастычным патэнцыялам для холангиокарциномы і аденокарциномы падстраўнікавай залозы, якія амаль немагчыма дыягнаставаць на ранняй стадыі сучаснымі метадамі скрынінга32,47.Здольнасць выяўляць рэдкія віды раку з дапамогай UCOM можа быць выкарыстана з цыркулявалай ДНК пухліны (ctDNA) з дапамогай палепшанай платформы для вадкаснай біяпсіі48.Даследаванне з выкарыстаннем панэлі выяўлення раку на аснове ДНК плазмы дало адчувальнасць 57,9%49.Нягледзячы на высокую спецыфічнасць, агульная прадукцыйнасць паказвае, што яшчэ ёсць што для паляпшэння.
Унікальныя характарыстыкі UCOM таксама падтрымліваюць даследаванне патэнцыялу UCOM у ацэнцы эфектыўнасці лячэння і маніторынгу рэцыдываў.У адпаведнасці з Крытэрыямі ацэнкі адказу пры салідных пухлінах (RECIST), медыцынская візуалізацыя з'яўляецца рэкамендаванай метадалогіяй для маніторынгу рэцыдываў і ацэнкі эфектыўнасці лячэння, у той час як опухолевые маркеры выкарыстоўваюцца толькі для ацэнкі50.У рэчаіснасці, аднак, на падыходы візуалізацыі ў значнай ступені ўплываюць частата і час, і таму пацыенты падвяргаюцца большай рызыцы і выдаткам51,52.Было пацверджана, што SIX6 служыць прэдыктарам метастазаў рака малочнай залозы32.Маніторынг ктДНК на аснове вадкай біяпсіі дазваляе ў рэжыме рэальнага часу назіраць за мінімальнымі рэшткавымі захворваннямі за некалькі месяцаў да рэнтгеналагічнага выяўлення, у ідэале затрымліваючы і прадухіляючы прагрэсаванне рака, звязанае з рэцыдывам53.Папярэднія вынікі сведчаць аб тым, што UCOM адлюстроўваюць узровень ракавага гиперметилирования ў рэжыме рэальнага часу адразу пасля аперацыі і лячэння32.Высокая адчувальнасць, якую дэманструюць UCOM, і магчымасць прымянення ў некалькіх неінтрузіўных тыпах узораў дазваляе UCOM служыць дакладным біямаркерам для маніторынгу рэцыдываў, захоўваючы пры гэтым высокую згоду пацыентаў.
У той жа час даступнасць тэсту для насельніцтва з'яўляецца яшчэ адной важнай праблемай, якая патрабуе дадатковых намаганняў.У той час як супрацоўніцтва UCOM па выяўленні было прынята ў большай колькасці бальніц у надзеі прынесці карысць большай колькасці пацыентаў, у сельскай мясцовасці Кітая актыўна праводзіліся бясплатныя выяўлення і скрынінгі.UCOM патрабуе палепшанай даступнасці, каб кваліфікавацца як магчымы інструмент праверкі, асабліва для слабаразвітых раёнаў.
У той час як вынікі прымянення UCOM у раннім выяўленні шматспадзеўныя, існуе шмат невядомых пра UCOM.Пры актыўным даследаванні неабходныя дадатковыя даследаванні таго, чаму UCOM паўсюдна прысутнічаюць у ракавых захворваннях.Асноўныя механізмы эпігенетычнай рэгуляцыі, якія ляжаць у аснове UCOM, заслугоўваюць далейшага даследавання, якое можа апраўдаць новы кірунак для лячэння рака.Вяртаючыся да ўзаемасувязі паміж гамагеннасцю і гетэрагеннасцю пухліны, нас цікавіць, чаму UCOM могуць быць выключэннем з большасці біямаркераў рака, якія цесна звязаны з пэўнымі тыпамі рака.Роля ідэнтыфікаваных UCOM аберацый метылявання ДНК у пухлінагенезе, прагрэсаванні пухліны і метастазах не была вызначана ў працэсе страты і аднаўлення клетачнай ідэнтычнасці і патрабуе дбайнага абследавання.Іншая вялікая цікавасць заключаецца ў аб'ёме ўключэння прыкметы гамагеннасці UCOM з унікальнымі для тканіны маркерамі ў надзеі наблізіцца да дакладнага выяўлення слядоў рака і ідэнтыфікацыі паходжання пухліннай тканіны ў зваротным парадку.UCOM можа быць ідэальным інструментам для прафілактыкі рака, выяўлення раку, а таксама патэнцыйнай абароны і ліквідацыі рака.
Грантавая падтрымка
Гэтая праца была падтрымана Кітайскай нацыянальнай ключавой праграмай даследаванняў і распрацовак (грант № 2022BEG01003), Нацыянальным фондам натуральных навук Кітая (гранты № 32270645 і 32000505), грантам Камісіі аховы здароўя правінцыі Хэйлунцзян (грант № 2020-111) , і грант Інстытута навукі і тэхналогій Хэзэ (грант № 2021KJPT07).
Заява аб канфлікце інтарэсаў
Вэй Лі з'яўляецца дырэктарам па даследаваннях і распрацоўках Shanghai Epiprobe Biotechnology Co., Ltd. Вэньцян Ю ўваходзіць у навукова-кансультатыўны савет Epiprobe.W. Yu і Epiprobe зацвердзілі патэнты, якія знаходзяцца на разглядзе гэтай працы.Усе іншыя аўтары заяўляюць аб адсутнасці канкуруючых інтарэсаў.
Аўтарскі ўклад
Задумалі і распрацавалі праект: Чэнчэнь Цянь і Вэньцян Ю.
Напісаў артыкул: Chengchen Qian.
Зрабіў ілюстрацыі: Chengchen Qian.
Рэцэнзавалі і рэдагавалі рукапіс: Сяолун Цзоу, Вэй Лі, Іньшань Лі і Вэньцян Ю.
Спасылкі
1. Сунг Х, Ферлей Дж, Зігель Р.Л., Лаверсан М, Соерджаматарам І, Джэмал А і інш.Сусветная статыстыка рака 2020: ацэнкі GLOBOCAN
захворванне і смяротнасць ва ўсім свеце ад 36 відаў раку ў 185 краінах.CA Cancer J Clin.2021 год;71: 209-49.
2. Ся С, Донг Х, Лі Х, Цао М, Сун Д, Хэ С і інш.Статыстыка рака ў Кітаі і Злучаных Штатах, 2022: профілі, тэндэнцыі і дэтэрмінанты.Chin MedJ (англ.).2022 год;135: 584-90.
3. Зігель Р.Л., Мілер К.Д., ВаглеНС, ДжэмалА.Статыстыка рака, 2023. CA Cancer J Clin.2023 год;73: 17-48.
4. Кросбі D, BhatiaS, Brindle KM, Coussens LM, Dive C, Emberton M і інш.Ранняе выяўленне рака.Навука.2022 год;375: eaay9040.
5. Ladabaum U, Дамініц JA, KahiC, Schoen RE.Стратэгіі для
скрынінг колоректального рака.Гастраэнтэралогіі.2020 год;158: 418-32.
6. Тануэ Л.Т., Танер Н.Т., Гулд М.К., Сільвестры Г.А.Скрынінг рака лёгкіх.Am J Respir Crit Care Med.2015 год;191: 19-33.
7. Bouvard V, WentzensenN, Mackie A, Berkhof J, BrothertonJ, Giorgi-Rossi P, et al.Погляд IARC на скрынінг рака шыйкі маткі.N EnglJ Med.2021 год;385: 1908-18.
8. Сюэ П, Нг МТА, Цяой.Праблемы кольпаскапіі для скрынінга рака шыйкі маткі ў краінах з нізкім узроўнем жыццядзейнасці і рашэнні штучнага інтэлекту.BMC Med.2020 год;18: 169.
9. Джонсан П, Чжоу Кю, Дао Д.Й., Ло Ю.М.Д.Цыркулюючыя биомаркеры ў дыягностыцы і лячэнні гепатоцеллюлярную карцынома.Nat Rev Gastroenterol Hepatol.2022 год;19: 670-81.
10. Van PoppelH, Albreht T, Basu P, HogenhoutR, CollenS, Roobol M. Сыроватачны ПСА на аснове ранняга выяўлення рака прастаты ў Еўропе і ва ўсім свеце: мінулае, сучаснасць і будучыня.Нацрэв.2022 год;19:
562-72.
11. Холіоаке А, О'Саліван П, Полак Р, Бест Т, Ватанабэ Дж, Кадзіта І,
і інш.Распрацоўка мультыплекснага аналізу РНК мачы для выяўлення і стратыфікацыі пераходна-клеткавага рака мачавой бурбалкі.Clin Cancer Res.2008 год;14: 742-9.
12. Фейнберг А. П., Фогельштэйн Б. Гіпаметыляванне адрознівае гены некаторых ракавых захворванняў чалавека ад іх звычайных аналагаў.Прырода.1983 год;301: 89-92.
13. Ng JM, Ю. Дж. Прамоўтэр гиперметилирования генаў-супрессоров пухліны ў якасці патэнцыйных биомаркеров колоректального рака.IntJ Mol Sci.2015 год;16: 2472-96.
14. Esteller M. Эпігеноміка рака: метиломы ДНК і карты мадыфікацыі гістонаў.Nat Rev Genet.2007 год;8: 286-98.
15. Нісіяма А, Наканішы М. Навігацыя ў ландшафте метилирования ДНК рака.Тэндэнцыі Genet.2021 год;37: 1012-27.
16. Се У, доктар медыцынскіх навук Шульц, ЛістэрР, Хоу З, Раджагопал Н, Рэй П і інш.Эпігеномны аналіз шматлінейнай дыферэнцыяцыі эмбрыянальных ствалавых клетак чалавека.Сотавы.2013 год;153: 1134-48.
17. Li Y, Zheng H, Wang Q, Zhou C, WeiL, Liu X і інш.Геномны аналіз паказвае ролю Polycomb у садзейнічанні гіпаметыляванню далін метылявання ДНК.геному Biol.2018 год;19:18.
18. Koch A, JoostenSC, Feng Z, de Ruijter TC, DrahtMX, MelotteV,
і інш.Аналіз метылявання ДНК пры раку: перагляд месца.Nat Rev Clin Oncol.2018 год;15: 459-66.
19. KleinEA, Richards D, Cohn A, TummalaM, Lapham R, Cosgrove D і інш.Клінічная праверка тэсту на ранняе выяўленне некалькіх ракавых захворванняў на аснове мэтанакіраванага метылявання з выкарыстаннем незалежнага набору праверкі.Эн Онкол.2021 год;32: 1167-77.
20. Ханахан Д, Вайнберг Р.А.Прыкметы рака.Сотавы.2000 год;100: 57-70.
21. Ханахан Д. Характэрныя прыкметы рака: новыя вымярэнні.Рак Discov.2022 год;12: 31-46.
22. Шварцберг Л, Кім Э.С., Лю Д., Шраг Д. Дакладная анкалогія: хто, як, што, калі і калі не?Am Soc Clin Oncol Навучальная кніга.2017: 160-9.
23. Лю Х, Мэн Х, Ван Дж. Колькаснае метилирование ў рэальным часе
выяўленне гена PAX1 пры скрынінгу рака шыйкі маткі.IntJ Gynecol Cancer.2020 год;30: 1488-92.
24. Imperiale TF, RansohoffDF, Itzkowitz SH, Levin TR, Lavin P, Lidgard GP і інш.Мультытаргетавае даследаванне ДНК для скрынінга колоректального рака.N EnglJ Med.2014 год;370: 1287-97.
25. Лі Дж, Лі І, Лі У, Ло Х, Сі І, Донг С і інш.Пазіцыянаванне кіраўніцтва
секвенирование вызначае аберрантныя шаблоны метылявання ДНК, якія змяняюць ідэнтычнасць клетак і сеткі назірання за імуннай пухлінай.Геном
Рэз.2019 год;29: 270-80.
26. Gao Q, LinYP, Li BS, Wang GQ, Dong LQ, Shen BY і інш.Ненадакучлівае выяўленне множных ракавых захворванняў шляхам секвеніравання метылявання цыркулюючай бясклетачнай ДНК (THUNDER): распрацоўка і незалежныя даследаванні праверкі.Эн Онкол.2023 год;34: 486-95.
27. Dong S, Li W, Wang L, Hu J, Song Y, Zhang B і інш.Гены, звязаныя з гістонамі, гіперметыляваны пры раку лёгкіх і гіперметыляваны
HIST1H4F можа служыць біямаркерам рака.Cancer Res.2019 год;79: 6101-12.
28. HeijnsdijkEA, Wever EM, AuvinenA, Hugosson J, Ciatto S, Nelen V, et al.Якасць жыцця эфекты скрынінга прастат-спецыфічнага антыгена.N EnglJ Med.2012 год;367: 595-605.
29. LuzakA, Schnell-Inderst P, Bühn S, Mayer-Zitarosa A, Siebert U. Клінічная эфектыўнасць тэстаў на біямаркеры скрынінга рака, прапанаваных у якасці самааплатнай службы аховы здароўя: сістэматычны агляд.Eur J грамадскага аховы здароўя.2016 год;26: 498-505.
30. Dong S, Lu Q, Xu P, Chen L, Duan X, Mao Z і інш.
Гіперметыляваны PCDHGB7 як універсальны толькі маркер рака і яго прымяненне ў раннім скрынінгу рака шыйкі маткі.Clin Transl Med.2021 год;11: e457.
31. Юань Дж, Мао Цы, Лу Цы, Сюй П, Ван С, Сюй Х і інш.Гиперметилированный PCDHGB7 як биомаркер для ранняга выяўлення рака эндаметрыя ў узорах шчотак эндаметрыя і соскобах з шыйкі маткі.Front Mol Biosci.2022 год;8: 774215.
32. Dong S, Yang Z, Xu P, Zheng W, Zhang B, Fu F і інш.Узаемна
эксклюзіўная эпігенетычная мадыфікацыя SIX6 з гиперметилированием для адсочвання з'яўлення метастазаў і предраковой стадыі.Перадача сігналу Target Ther.2022 год;7: 208.
33. Huang L, Guo Z, Wang F, Fu L. KRAS мутацыя: ад нелекарства да лекаў пры раку.Перадача сігналу Target Ther.2021 год;6: 386.
34. Бялінскі SA, Nikula KJ, PalmisanoWA, MichelsR, SaccomannoG, GabrielsonE і інш.Аберрантнае метыляванне p16(INK4a) з'яўляецца ранняй падзеяй пры раку лёгкіх і патэнцыйным біямаркерам для ранняй дыягностыкі.Proc Natl Acad Sci U SA.1998 год;95: 11891-6.
35. Робертсан К.Д.Метыляванне ДНК і хваробы чалавека.Nat Rev Genet.2005 год;6: 597-610.
36. WentzensenN, Walker JL, Gold MA, Smith KM, ZunaRE,
Mathews C і інш.Множныя біяпсіі і выяўленне папярэднікаў рака шыйкі маткі пры кольпоскопіі.J Clin Oncol.2015 год;33: 83-9.
37. Дэ Штрупер Л.М., Мейер Ч.Дж., Беркхоф Дж., Хесселінк А.Т., Снайдэрс
PJ, Steenbergen RD і інш.Аналіз метилирования FAM19A4
ген у саскобах шыйкі маткі вельмі эфектыўны ў выяўленні шыйкі маткі
карцынома і запушчаныя паразы CIN2/3.Рак Prev Res (Phila).2014 год;7: 1251-7.
38. Тайская А.А., Саламон Б.Дж., Секвіст Л.В., Гейнор Дж.Ф., Хіст Р.С.Рак лёгкіх.Ланцэт.2021 год;398: 535-54.
39. Grunnet M, Sorensen JB.Карциноэмбриональный антыген (СЕА) у якасці опухолевого маркера пры раку лёгкіх.Рак лёгкіх.2012 год;76: 138-43.
40. Вуд DE, KazerooniEA, Baum SL, EapenGA, EttingerDS, Hou L і інш.Скрынінг рака лёгкіх, версія 3.2018, NCCN Clinical Practice Guidelines in Oncology.J Natl Compr Canc Netw.2018 год;16: 412-41.
41. Амерыканскае таварыства рака.Факты і лічбы пра рак.Атланта, Джорджыя, ЗША: Амерыканскае таварыства рака;2023 [абноўлена 1 сакавіка 2023 г.;цытуецца 22 жніўня 2023 г.].
42. FonthamETH, Wolf AMD, Church TR, EtcioniR, Flowers CR,
Герцыг А і інш.Скрынінг на рак шыйкі маткі для асоб з сярэдняй рызыкай: абнаўленне рэкамендацый Амерыканскага таварыства рака на 2020 год.CA Cancer J Clin.2020 год;70: 321-46.
43. Clarke MA, Long BJ, Del Mar MorilloA, Arbyn M, Bakkum-Gamez JN, Wentzensen N. Асацыяцыя рызыкі рака эндаметрыя з крывацёкам у постменопаузе ў жанчын: сістэматычны агляд і метааналіз.JAMA Intern Med.2018 год;178: 1210-22.
44. Якабс I, Джентры-Махарадж А, Бернэл М, Манчанда Р, Сінгх Н,
Шарма А і інш.Адчувальнасць трансвагінальном ультрагукавога скрынінга
для рака эндаметрыя ў жанчын у постменопаузе: даследаванне выпадак-кантроль у кагорце UKCTOCS.Ланцэт Анкол.2011 год;12: 38-48.
45. BabjukM, Burger M, CompératEM, Gontero P, MostafidAH,
PalouJ і інш.Кіраўніцтва Еўрапейскай асацыяцыі ўралогіі па неінвазіўным раку мачавой бурбалкі (TaT1 і карцынома in situ) -
Абнаўленне 2019.Еўра Урол.2019 год;76: 639-57.
46. Арагон-Чынг Дж.Б.Праблемы і дасягненні ў дыягностыцы, біялогіі і лячэнні карцынома верхняга аддзела уротелия і мачавой бурбалкі.Урол Анкол.2017 год;35: 462-4.
47. Rizvi S, KhanSA, Hallemeier CL, Kelley RK, Gores GJ.
Холангиокарцинома - развіваюцца канцэпцыі і тэрапеўтычныя стратэгіі.Nat Rev Clin Oncol.2018 год;15: 95-111.
48. Ye Q, Ling S, Zheng S, Xu X. Вадкая біяпсія гепатацэлюлярнай
карцынома: цыркулююць опухолевые клеткі і цыркулююць опухолевые ДНК.Мол рак.2019 год;18: 114.
49. Чжан І, Яо І, Сюй І, Лі Л, Гун І, Чжан К і інш.Пан-рак
выяўленне ДНК цыркулявалай пухліны ў больш чым 10 000 кітайскіх пацыентаў.Нац камун.2021 год;12:11.
50. Eisenhauer EA, Therasse P, BogaertsJ, Шварц LH, Sargent D, Ford R і інш.Новыя крытэрыі ацэнкі адказу пры салідных пухлінах: перагледжанае кіраўніцтва RECIST (версія 1.1).Eur J Рак.2009 год;45: 228-47.
51. LitièreS, Collette S, de Vries EG, Seymour L, BogaertsJ.RECIST - вучыцца на мінулым, каб будаваць будучыню.Nat Rev Clin Oncol.
2017 год;14: 187-92.
52. Сеймур Л., Багартс Дж., Перроне А., ФордР., Шварц Л.Х., Мандрэкар С. і інш.iRECIST: рэкамендацыі па крытэрыях адказу для выкарыстання ў выпрабаваннях
тэставанне імунатэрапеўтычных сродкаў.Ланцэт Анкол.2017 год;18: e143-52.
53. PantelK, Alix-Panabières C. Вадкая біяпсія і мінімальная рэшткавая хвароба - апошнія дасягненні і наступствы для лячэння.Nat Rev Clin Oncol.2019 год;16: 409-24.
Цытуйце гэты артыкул як: Qian C, Zou X, Li W, Li Y, Yu W. Фарпост супраць рака: універсальныя толькі маркеры рака.Рак Biol Med.2023 год;20: 806-815.
doi: 10.20892/j.issn.2095-3941.2023.0313
Час размяшчэння: 7 мая 2024 г